CIENCIAS BIOLÓGICAS Y DE LA SALUD
Aprueban el uso de un nuevo test molecular de COVID-19, sensible, específico, rápido y económico
Investigadores del CONICET lideraron el desarrollo que se encuentra enmarcado en la Unidad Coronavirus COVID-19.
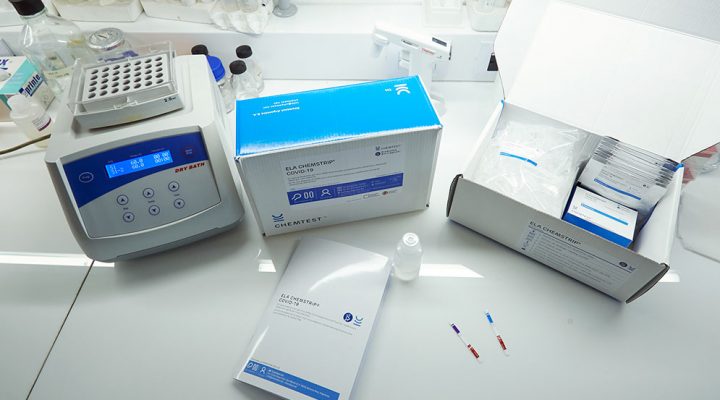
Científicos argentinos desarrollaron un nuevo test de COVID-19 de base molecular, rápido, de bajo costo y fácil de maniobrar, que fue recientemente aprobado por la Administración Nacional de Medicamentos Alimentos y Tecnología Médica (ANMAT). El kit de diagnóstico fue bautizado como ELA-CHEMSTRIP.
ELA-CHEMSTRIP no sólo posibilita detectar el genoma del Coronavirus SARS-CoV-2 en muestras de ARN, con similar sensibilidad y especificidad que la reacción en cadena de la polimerasa con transcripción inversa (RT-PCR, por sus siglas en inglés)- técnica de referencia usada por el ANLIS/Malbrán y los centros descentralizados-, sino que también permite acortar los tiempos, reducir costos (dado que el equipamiento que requiere es menos sofisticado, más económico e implica un porcentaje menor de insumos importados) y no necesita ser maniobrado por personal altamente calificado. Por otro lado, al igual que RT-PCR, el nuevo kit permite hacer un diagnóstico temprano de COVID-19.
El proyecto de desarrollo, enmarcado en la Unidad Coronavirus COVID-19 (creada en conjunto por el MINCyT, el CONICET y la Agencia I+D+i), es producto de una asociación entre la Universidad Nacional de San Martín (UNSAM), la Universidad Nacional de Quilmes (UNQUI) y las empresas de base tecnológica CHEMTEST y Productos Bio-lógicos SA (PB-L). Diego Comerci, investigador del CONICET en el Instituto de Investigaciones Biotecnológicas (IIBIO, CONICET-UNSAM) y socio de CHEMTEST, y Marcos Bilen, investigador del Consejo en el Laboratorio de Ingeniería Genética y Biología Molecular y Celular (LIGBCM, UNQUI) y parte de PB-L, lideraron el desarrollo.
Las pruebas de validación de ELA-CHEMSTRIP, hechas a partir de paneles de muestras de ARN aportadas por el ANLIS/Malbrán, mostraron cerca de un 96 por ciento de sensibilidad (es decir, arrojaron muy pocos falsos negativos) y un 100 por ciento de especificidad, lo que significa que no hubo ningún falso positivo. Es importante destacar que las muestras positivas tenían distintos niveles de carga viral y correspondían tanto a pacientes sintomáticos como asintomáticos.
Una solución integral para el trabajo en territorio
El proceso de diagnóstico de COVID-19 mediante un técnica de base molecular como RT-PCR implica fundamentalmente tres etapas: 1) Extracción de una muestra respiratoria mediante un hisopado nasofaríngeo, que es seguida, en caso de que el centro en el que se la realiza no cuente con cabinas de bioseguridad adecuadas, por una compleja logística de traslado 2) Aislamiento o purificación del ARN a partir del hisopado 3) Testeo para detectar fehacientemente el material genético del virus en la muestra de ARN.
En un país extenso como la Argentina en un contexto de una pandemia, la posibilidad de garantizar testeos a todos aquellos que lo necesiten podría implicar dificultades económicas, de tiempo, infraestructurales, logísticas y hasta de acceso a recursos que necesitan importarse y tienen una alta demanda global.
El desafío que se plantaron los equipos de investigación en marzo de este año, cuando comenzaron a trabajar de forma conjunta con el propósito de poder integrar sus distintas experticias y conocimientos, fue dar respuestas a los problemas que implican cada una de las fases mencionadas.
“La idea que nos propusimos fue armar un sistema integral de detección de SARS-CoV-2 que sea simple de implementar y que se pueda realizar en el territorio, es decir, en centros de atención de baja complejidad, unidades móviles o incluso en laboratorios de campañas, que no cuentan con equipamientos sofisticados y costosos como un equipo de RT-PCR”, afirma Diego Comerci.
“Lo que hicimos fue pensar soluciones para cada una de las etapas con el fin de bajar los costos, disminuir los tiempos y ampliar las posibilidades de acceso al diagnóstico. Esto también sirve para descomprimir la demanda que existe sobre los centros de referencia que utilizan RT-PCR”, agrega Marcos Bilen.
En cuanto a la primera etapa, actualmente se encuentran trabajando en la posibilidad de colocar el hisopado sobre una solución que inactive el virus y permita evitar las complejas medidas de seguridad que requiere su traslado a centros alejados con las cabinas de bioseguridad necesarias. Respecto de la segunda, los investigadores ya cuentan con un kit de extracción de ARN viral que podría acompañar el uso de ELA-CHEMSTRIP, que es, justamente, una alternativa a la necesidad utilizar equipos de RT-PCR en la tercera fase.
Una tecnología sensible y específica
ELA-CHEMSTRIP está basado en una tecnología molecular de detección viral directa conocida como ELA (Easy Loop Amplification), que permite reconocer regiones específicas del genoma del SARS-COV-2 en una muestra de ARN.
Al igual que RT-PCR y la amplificación isotérmica mediada por bucle (LAMP, por sus siglas en inglés), ELA funciona bajo el principio de multiplicar el número de copias de pequeños fragmentos de ADN o ARN, como los que se aíslan de las muestras respiratorias tomadas a los pacientes mediante hisopados, para posibilitar su detección.
“ELA es una tecnología de amplificación isotérmica del genoma desarrollada en conjunto por el LIGBCM y PB-L que, a diferencia de LAMP, funciona a partir de enzimas producidas íntegramente en la Argentina, aisladas de bacterias autóctonas, e incorpora componentes que hacen que sea mucho más específica que aquella, lo que reduce la posibilidad de arrojar falsos positivos”, señalas Bilen.
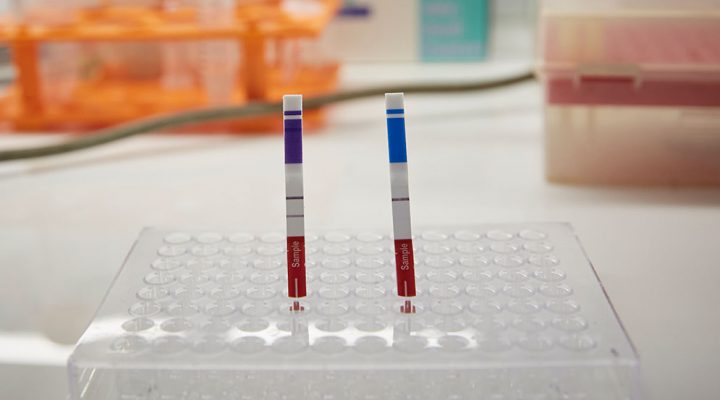
La amplificación de regiones específicas del genoma viral se conjuga con un método de visualización. En el caso de ELA-CHEMSTRIP se trata del sistema inmunocromoatgrafico bajo la forma de tiras reactivas de papel, en cuyo desarrollo y producción tiene amplia experiencia el consorcio conformado por el IIBIO y CHEMTEST.
“Estos test funcionan en base a anticuerpos específicos que inmunocapturan las moléculas virales amplificadas en la reacción anterior –en caso de que en la muestra contuviera el material genético del virus- y señalizan el resultado a través de bandas de color en una tira de papel (como las pruebas de embarazo). ELA-CHEMSTRIP cuenta con dos anticuerpos que sólo reconocen al producto amplificado correcto”, señala Diego Comerci.
Una vez que se tiene aislada la muestra de ARN que se desea analizar, el procedimiento es sencillo. En primer lugar, la muestra es colocada en un tubo de reacción, junto con un complejo de enzimas, primers y sondas, e incubada a 60 grados durante cerca de 45 minutos. En este paso, al ARN se retrotranscribe en ADN y, sólo en caso de que el material genético del SARS-CoV-2 esté presente, se multiplican exponencialmente las copias de determinadas regiones del genoma viral. Luego se pone la tira reactiva de papel sobre la solución (dentro del tubo de reacción) y se espera hasta diez minutos. Si al extraer la tira, ésta muestra dos bandas coloreadas, significa que el paciente tiene COVID-19, si, en cambio, solo exhibe una franja de color, eso quiere decir que no está infectado con SARS-CoV-2.
Un desafío productivo
Comerci y Bilen coinciden en señalar que el mayor desafió que implicaba este trabajo conjunto no era a nivel del desarrollo, dado que de lo que se trataba era de readecuar e integrar tecnologías de amplificación y visualización que ya habían probado en otros test y en las que contaban con sobrada experiencia, sino de garantizar que se pudieran producir a gran escala en la Argentina. La capacidad instalada de CHEMTEST para fabricar tiras reactivas de papel inmunocromatográficas es clave para que esto sea posible.
“De otra forma, el desarrollo no hubiera tenido sentido, al no ofrecer una verdadera solución a un problema de salud pública, como lo es el de garantizar un mayor acceso al diagnóstico de COVID-19 en el marco de la pandemia”, advierte Bilen.
La idea es producir mensualmente alrededor de 100 mil unidades del kit. La primera partida, actualmente en proceso, va a ser de 50 mil unidades, pero se estima que para el próximo mes se van a fabricar 130 mil determinaciones.
“Esto fue posible gracias al apoyo y la coordinación múltiples estamentos del Estado. En este sentido, en primer lugar, quisiera destacar el rol del MINCyT, y especialmente las gestiones de su Secretario de Articulación Científico-Tecnológica, Juan Pablo Paz, para reestablecer el funcionamiento adecuado del ROECyT (Registro de Organismos y Entidades Científicas y Tecnológicas), gracias a lo cual pudimos ingresar veinte órdenes de compra al exterior en un solo mes. Además, me gustaría agradecer la colaboración de Aerolíneas Argentinas, cuyos aviones sanitarios nos permitieron traer insumos clínicos de China y también repatriar investigadores que habían quedado varados en Alemania y Colombia. Tampoco puedo dejar de mencionar la colaboración que recibimos de AFIP, Aduana, Jefatura de Gabinete, Cancillería, ANLIS/Malbrán y SENASA”, concluye Comerci.
Por Miguel Faigón
Sobre investigación
IIBIO (CONICET-UNSAM)/CHEMTEST
Diego Comerci. Investigador principal.
Juan Ugalde. Investigador principal.
Andrés Ciocchini. Investigador adjunto.
Luciano Melli. Investigador asistente.
Josefina Caillava. Becaria posdoctoral.
Stella Maris Landívar. Becaria doctoral.
Tamara Laube
Agustina Carreño.
LIGBCM (UNQUI)/ PB-L
Marcos Bilen. Investigador adjunto.
Daniel Ghiringhelli. Investigador principal.
Cristina Borio. Investigadora asistente.
Julián Bergier. Becario doctoral.
Lucas Ripoll. Becario doctoral.
Victoria Nugnes. Becaria doctoral.
Lorena Rojas. Investigadora adjunta.
Yamila Santillán. Becaria posdoctoral.
Damián Presti. Becario posdoctoral.
Ana Ventura.
Vanina Rodriguez
Cristian Mobilia
Marcelo Romero
Melisa Da Silva.