CIENCIAS EXACTAS Y NATURALES
Ver para creer: nanoscopía de fluorescencia
Un breve recorrido por la historia de la microscopía desde sus orígenes hasta el desarrollo de las técnicas actuales de cada vez mayor resolución
Por Fernando Stefani *
Infinidad de procesos y fenómenos son invisibles al ojo humano. Para estudiarlos y descifrar el funcionamiento de la naturaleza, los científicos debemos muchas veces basarnos en evidencias indirectas. Sin embargo, no estamos exentos del inigualable poder de convicción de las imágenes. Debe ser por ello que todas las variantes de microscopía despiertan en científicos y no científicos tanta fascinación y han dado lugar a importantes descubrimientos. No es casual tampoco que casi todas las modalidades de microscopía hayan motivado un Premio Nobel.
La microscopía óptica fue la primera en desarrollarse a partir de la invención de las primeras lupas que permitieron obtener imágenes magnificadas de un objeto. Pero resulta que existe un límite, conocido como el límite de resolución de un microscopio o barrera de difracción, que no permite visualizar los detalles de un objeto por debajo de un cierto tamaño. El físico alemán Ernst Abbe fue quien en 1873 identificó los fundamentos físicos de este límite, y demostró que su origen se encuentra en la naturaleza ondulatoria de la luz. Típicamente el límite de resolución toma valores de media longitud de onda, es decir unos 250 nm para la luz visible.
Pero, ¿por qué querríamos ver cosas más pequeñas? Un particular interés surge del estudio de sistemas biológicos. A nivel macroscópico, con dimensiones de cm o mm, se tienen órganos y tejidos, los cuales a su vez están compuestos de diversos tipos de células que tienen dimensiones del orden de los micrómetros (1 µm= 0,001 mm). Hasta aquí todo puede visualizarse con microscopios ópticos tradicionales. Pero más profundamente existe toda una maquinaria biofisicoquímica de organización y estructuración interna de las células, así como procesos de comunicación e interacción entre células, que tienen lugar en la escala de los nanómetros (1 nm = 0,001 µm), cuyos detalles permanecen ocultos detrás de la barrera de difracción.
Para sortear este obstáculo se desarrollaron microscopios basados en otros principios físicos, como el microscopio electrónico que consigue resoluciones menores a 1 nm, pero requiere que las muestras estén en vacío, resistan y den contraste tras el bombardeo de electrones, algo que dificulta enormemente la observación directa de tejido o células vivas. Otra familia de microscopías que ofrecen resolución nanométrica son las de sondeo superficial, como la de fuerza atómica, pero están limitadas a observar la superficie de especímenes.
Es por esto que las diversas variantes de microscopía óptica siguen vigentes. La luz visible es poco o nada dañina, y permite observar el interior de células y tejidos. Numerosos desarrollos tecnológicos del siglo XX mejoraron los microscopios ópticos. El láser y el microscopio confocal convirtieron a la microscopía óptica de fluorescencia en la herramienta principal de visualización de estructuras y procesos biológicos. La microscopía de fluorescencia permite marcar específicamente lo que uno quiere ver y brinda enorme sensibilidad -es posible detectar la luz emitida por una sola molécula-. La cantidad de información que se ha obtenido mediante la microscopía de fluorescencia es inmensa, pero como cualquier variante de óptica no escapa al límite de difracción.
Hasta hace tan solo dos décadas, la barrera de difracción parecía inquebrantable. Pero en 1994, Stefan W. Hell, colaborador nuestro y ganador del Premio Nobel de Química 2014, abrió una puerta que llevó al desarrollo de las denominadas microscopías de súper-resolución o nanoscopías de fluorescencia. Estas metodologías ofrecen en teoría resolución ilimitada. En la práctica se han alcanzado resoluciones de 6 nm en muestras no biológicas, de unos 20 nm en células fijadas, y de entre 60 y 80 nm en células vivas o tejidos.
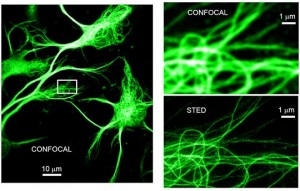
Comparación de una imagen confocal con una de súper-resolución por STED (stimulated emission depletion)./ Imagen: Gentileza investigador.
Un objetivo estratégico que nos hemos propuesto es el de convertir al Centro de Investigaciones en Bionanociencias (CIBION) en referente nacional en nanoscopías de fluorescencia. Para ello he establecido a través de un Partner Group de la Sociedad Max Planck, una colaboración estrecha con el departamento del Prof. Hell en el Instituto Max Planck de Biofisicoquímica (MPIbpc, Göttingen), donde dos becarios doctorales de mi grupo, Martín D. Bordenave y Federico Barabas, han realizado estadías de formación y entrenamiento.
Además, junto al Prof. Hell co-dirigimos un postdoc argentino, Francisco Balzarotti, que actualmente trabaja en el MPIbpc. En CIBION hemos construido dos microscopios con tecnología de punta a nivel internacional, que permiten aplicar distintas técnicas de nanoscopía de fluorescencia. Ambos microscopios se encuentran abiertos a toda la comunidad científica a través del Sistema Nacional de Microscopía del Ministerio de Ciencia, Tecnología e Innovación Productiva.
La aplicación de estas metodologías en Argentina tendrá un impacto particular. Nuestro país cuenta tradicionalmente con una comunidad científica especialmente fuerte en bioquímica, biología celular y biomedicina. Estoy convencido de que las nanoscopías de fluorescencia se convertirán en una herramienta clave para estas áreas, ya que habilitan la observación de procesos biológicos en una dimensión hasta ahora imposible, brindando información clave sobre el funcionamiento de organismos y enfermedades.
Nuestro objetivo es ampliar las posibilidades de nuestro laboratorio y ofrecer cada vez más y mejores posibilidades en este campo dando lugar a investigaciones argentinas interdisciplinarias de alto impacto internacional.
*Fernando Stefani es investigador independiente del CONICET, vice-director del Centro de Investigaciones en Bionanociencias “Elizabeth Jares Erijman” (CIBION-CONICET). Es profesor regular adjunto del Departamento de Física de la Facultad de Ciencias exactas y naturales, de la Universidad de Buenos Aires.