TECNOLOGÍA
Mejorar el diagnóstico de osteoporosis mediante herramientas de inteligencia artificial
Este es el objetivo de un proyecto de investigadores del CONICET escogido para su financiamiento por la empresa estadounidense Salesforce.
La osteoporosis es una enfermedad caracterizada por la disminución de la masa ósea y el deterioro de la microestructura de los huesos, con la concomitante incrementación de la fragilidad ósea y la predisposición a sufrir fracturas.
Actualmente, esta enfermedad se diagnostica a partir del cálculo de la densidad mineral ósea, valor que se obtiene a través de un en estudio conocido como absorciometría con rayos X de doble energía (DXA, por sus siglas en inglés). La densidad ósea es medida en todas las vértebras del paciente, y a través de una tabla estandarizada, que contempla también la edad y el sexo, se determina si el individuo tiene o no osteoporosis y si, por lo tanto, debe o no seguir un tratamiento médico. La limitación del estudio es que esta técnica solo permite describir, aproximadamente, hasta el 70 por ciento de la degradación ósea de una persona.
“Esta falta de precisión conduce a que alrededor de un 30 por ciento de las personas que son diagnosticadas con osteoporosis tengan que seguir un tratamiento que en realidad no necesitan, y que a un porcentaje similar de los individuos con osteoporosis que se hacen la DXA no se les detecte la enfermedad y no se les provea una terapia”, explica Felix Thomsen, investigador del CONICET en la Universidad Nacional del Sur (UNS).
Thomsen y Emmanuel Iarussi, investigador del CONICET en la Universidad Tecnológica Nacional (UTN), acaban de ser reconocidos con un subsidio de la empresa estadounidense Salesforce, como resultado de un concurso abierto para la presentación de proyectos vinculados al uso de inteligencia artificial (IA).
El proyecto que presentaron Iarussi y Thomsen, escogido para su financiamiento junto con otros cinco, entre más de 180 postulaciones provenientes de más de treinta países, apunta justamente a poder hacer más preciso el diagnóstico de osteoporosis mediante el uso de distintas técnicas de IA. Es la primera vez que investigadores argentinos reciben este subsidio.
Filtrar ruidos y aumentar datos mediante IA
La idea base del proyecto consiste en complementar la DXA con una tomografía computada (TC), que permita obtener mayor cantidad de parámetros estructurales de la geometría vertebral, y así poder optimizar el diagnóstico. El inconveniente es que las imágenes de TC de pacientes vivos todavía son de baja resolución y “muy ruidosas” como para poder obtener parámetros microestructurales, más allá de la densidad ósea.
“Lo que sucede es que aunque la densidad del hueso no es el único parámetro característico de la osteoporosis, es el único que por ahora puede medirse con confianza in vivo. Los otros parámetros son estructurales, pero para poder capturarlos se necesitan imágenes más detalladas. No obstante, estos otros parámetros se advierten en autopsias, por ejemplo, y si se extrae un hueso de una persona recientemente fallecida y se los escanea en alta calidad, es posible también observarlos en imágenes en 3D”, afirma Thomsen.
Es en este punto, para sortear las dificultades mencionadas, que las novedosas herramientas de IA pueden hacer importantes aportes. “La idea de base sería, a partir de lo que se conoce como redes neuronales convolucionales, entrenar a un algoritmo para que al mostrarle vértebras escaneadas en 3D en alta resolución pueda aprender a filtrar el ruido de las imágenes de más baja calidad, obtenidas mediante una TC en pacientes in vivo. Esto permitiría por primera vez medir in vivo la microarquitectura del hueso”, explica Thomsen.
Hace ya unos años que el trabajo de Thomsen se encuentra orientado en esta dirección. Pero la dificultad con la que se encuentra la propuesta es que para que resulte eficaz una técnica como la de las redes neuronales convolucionales, es necesario no solo desarrollar buenos algoritmos de base sino también disponer de muchos pacientes para entrenarlos, de forma tal que aprendan a filtrar los ruidos de imágenes de peor calidad.
El problema es que las imágenes de alta resolución que se necesitan para el entrenamiento sólo se pueden obtener a través del escaneo de huesos ex vivo de personas recientemente fallecidas, porque si pasan más de dos días se descomponen demasiado. Por diversas razones, conseguir estos tejidos óseos, para disponer de un set lo suficientemente amplio y robusto, resulta muy complicado.
“Entonces, surgió la idea de ver si podíamos generar artificialmente estructuras óseas sintéticas in silico que permitieran engrosar la base del entrenamiento del algoritmo de redes neuronales convolucionales”, relata Thomsen.
Es en este punto en el que la experticia de Iarussi en el desarrollo de estructuras sintéticas virtuales que lucen como reales y, más específicamente, su incursión en un método novedoso de IA, conocido como redes neuronales generativas antagónicas (GANs), se complementa con las necesidades de Thomsen.
“Si fuera posible tener decenas de miles de vértebras escaneadas en alta resolución, posiblemente no sería necesario nuestro aporte. Pero como son muy escasas, hay que ponerse creativo”, señala Iarussi, quien también es profesor adjunto en la Facultad de Ciencias Exactas y Naturales de la Universidad de Buenos Aires (FCEN, UBA).
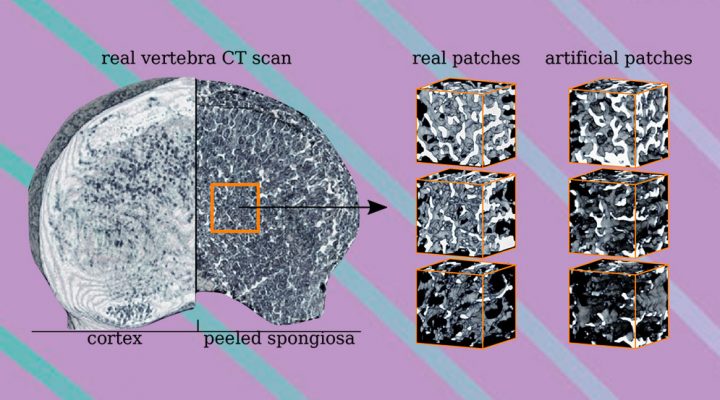
Lo que permiten las GANs es generar, a partir de no demasiados ejemplos -no más que unas pocas vértebras humanas escaneadas ex vivo, en este caso- , muchas estructuras sintéticas virtuales, que no sean idénticas a los escaneadas pero que a la vez luzcan como reales. Otro dato importante es que las estructuras generadas, aun con cierto margen para la aleatoriedad, se pueden parametrizar.
“Nosotros tenemos algunos huesos escaneados y, a partir de esa base, generamos artificialmente muchos más y controlamos ciertas características que queremos para cada uno. Así como ahora hay algoritmos que te permiten obtener, por ejemplo, la imagen de la cara de un hombre de 43 años de pelo oscuro y barba, que no sea real pero luzca como tal (lo que se conoce como deepfake), nosotros podemos crear huesos sintéticos que tengan determinados parámetros generales. Pero además, podemos pedirle que genere aleatoriamente muchos otros que cumplan con las mismas características y, al mismo tiempo, sean diferentes entre sí”, destaca Iarussi.
La ventaja con las que cuentan los algoritmos que aprenden a generar rostros humanos es que pueden contar con muchísimo ejemplos para hacer su entrenamiento y aprendizaje, mientras Iarussi y Thomsen solo tienen hasta ahora doce vértebras humanas escaneadas, lo que hace mucho más desafiante la tarea.
Los primeros y promisorios resultados de esta iniciativa fueron publicados en las actas de la International Conference on Medical Image Computing and Computer-Assisted Intervention y en la revista Computerized Medical Imaging and Graphics, ambos en el año 2020. De estos trabajos también formaron parte Claudio Delrieux, director tanto de Iarussi como de Thomsen e investigador del CONICET en la UNS, y otros investigadores de Argentina, Alemania y España.
“Se trata, hasta donde sabemos, del primer método para modelar artificialmente hueso y crear estructuras óseas virtuales. Pero además, para hacerlo, recurrimos a una técnica de IA muy novedosa en la que Emmanuel es especialista”, destaca Thomsen.
Obtener artificialmente más ejemplos de cómo pueden ser los huesos de la columna vertebral, a través de las GANs, permite aumentar la base de entrenamiento del algoritmo de redes neuronales convolucionales para optimizarlo y que pueda filtrar el ruido de las imágenes de TC.
Amén de los buenos resultados obtenidos hasta el momento, los investigadores recalcan que el estudio se encuentra todavía en una etapa exploratoria: “Es importante aclarar que, aunque ese es el objetivo final, todavía estamos lejos de poder ofrecer un diagnóstico o de que esto llegue a ser una aplicación clínica”, subraya Iarussi.
Por Miguel Faigón
Referencias bibliográficas
Iarussi E., Thomsen F., Delrieux C. (2020) Generative Modelling of 3D In-Silico Spongiosa with Controllable Micro-structural Parameters. In: Martel A.L. et al. (eds) Medical Image Computing and Computer Assisted Intervention – MICCAI 2020. MICCAI 2020. Lecture Notes in Computer Science, vol 12266. Springer, Cham. https://doi.org/10.1007/978-3-030-59725-2_76
Thomsen, F., Delrieux, C., Pisula, J., Fuertes García, J. M., Lucena, M., de Luis García, R., & Borggrefe, J. (2020). Noise reduction using novel loss functions to compute tissue mineral density and trabecular bone volume fraction on low resolution QCT. Computerized Medical Imaging and Graphics, 86, 101816. https://doi.org/10.1016/j.compmedimag.2020.101816