CONICET, Facultad de Medicina, UBA.
Científicos del CONICET investigan el vínculo entre el transporte axonal y las enfermedades neurodegenerativas
Una mala distribución del sistema de degradación de proteínas en neuronas podría estar asociado a diferentes patologías.
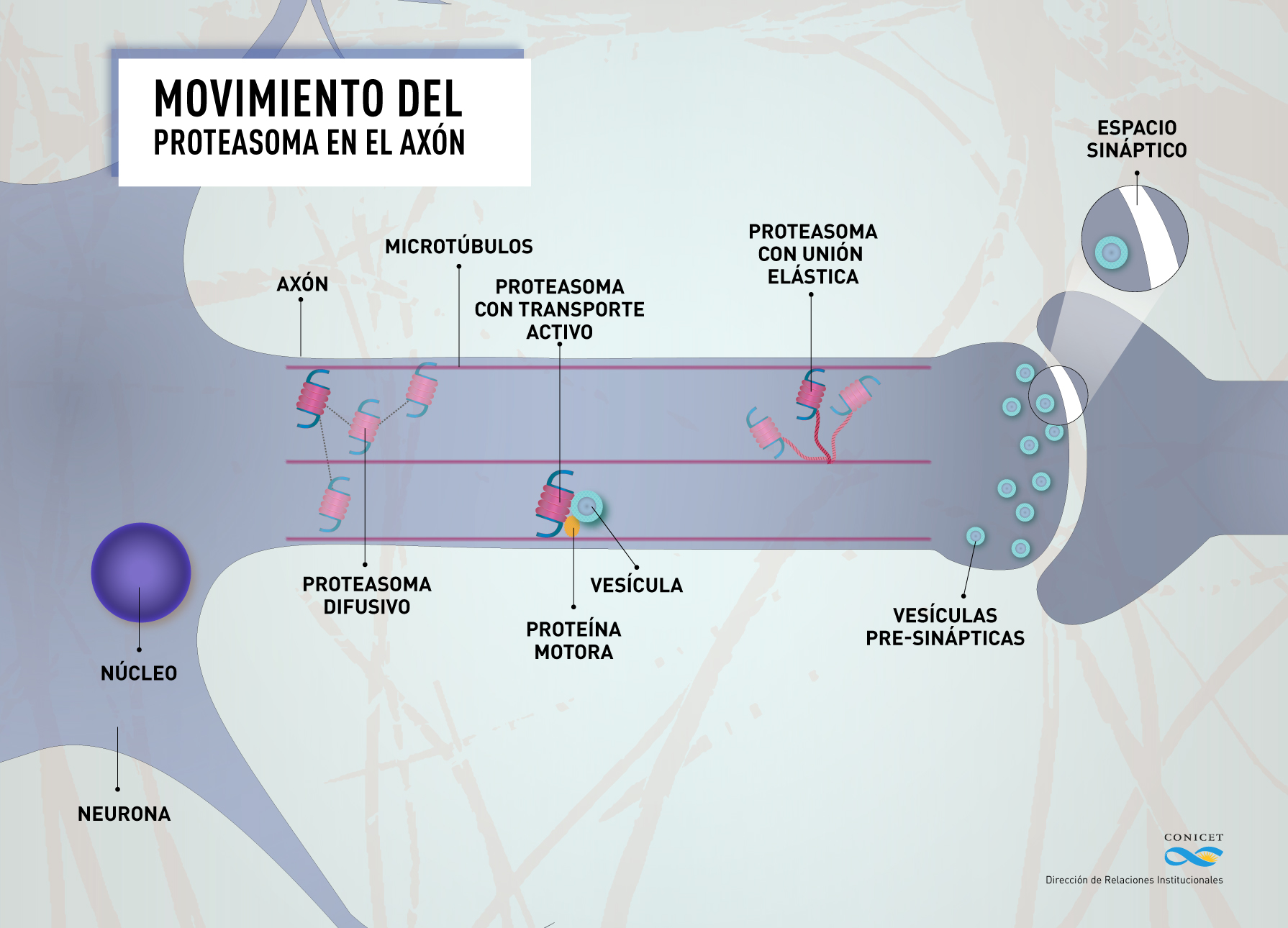
La trasmisión del impulso nervioso entre las neuronas depende en gran medida del correcto transporte a lo largo del axón de vesículas que contienen diferentes moléculas. El axón, una prolongación especializada en la conducción del estímulo desde el cuerpo celular hacia la sinapsis, es el puente de unión entre las neuronas que posibilita la transmisión del impulso y el arribo de vesículas encargadas de liberar neurotransmisores al espacio intercelular para transmitir la señal.
Sin embargo, una vez que ejercen su efecto, esas moléculas deben ser degradadas para prevenir su acumulación. Si ese proceso es defectuoso, podría afectar la señalización entre células. En ese campo Tomás Falzone, investigador adjunto del CONICET en el Instituto de Biología Celular y Neurociencias (IBCN, CONICET-UBA) centra su trabajo en los mecanismos de degradación de proteínas llevada a cabo específicamente por el sistema ubiquitina-proteasoma, una maquinaria compleja que se encarga de destruir aquellas proteínas que no sirven o simplemente señalizarlas para que sean desechadas a posteriori.
“La ubiquitina es una pequeña proteína que se encuentra en todas las células. Cuando muchas de estas se unen a otras proteínas que tienen que ser eliminadas, el proteasoma, que es como una gran máquina molecular con forma de barril provista de una tapa, se encarga de validar la ‘basura’, introducirla y destruirla en su interior”, explica Falzone.
Ahora bien, ¿Qué sucede cuando este barril que llamamos proteasoma no se encuentra presente donde debería? ¿Cómo es que ocurre su transporte en el axón de las neuronas y cómo los defectos en este proceso están relacionados con determinadas enfermedades?.
Éstas son solo algunas de las preguntas que tiene por objetivo contestar el grupo de investigación de Falzone, quien en su laboratorio estudió cómo se mueve este barril en diferentes lugares de la neurona.
Un barril en constante movimiento
Según el investigador, en algunas enfermedades neurodegenerativas como el Parkinson o el Alzheimer se produce, entre otros factores, la acumulación anormal de proteínas que no fueron degradadas.
“No se sabe bien porqué, si es que el sistema de degradación no funciona bien o porque no está presente en el lugar donde tiene que estar”, dice Falzone y agrega que ésta fue la incertidumbre disparadora de la hipótesis de su trabajo de investigación: ¿Es necesario que haya un sistema de transporte a lo largo de una célula tan polarizada y que distribuya el proteasoma en los lugares en que debe actuar?.
Es aquí donde es importante hablar de los microtúbulos, unas estructuras celulares largas en forma de tubos que forman el citoesqueleto, soportan el transporte de organelas y que dan el marco estructural de la célula. Para que ocurra el desplazamiento de vesículas de secreción, de organelas y del proteasoma no sólo son necesarios estos ‘tubos’ que harían de una suerte de carril, sino que también son imprescindibles las proteínas motoras que impulsan el movimiento.
“Esas proteínas funcionan como una especie de servicio postal, trasladando la carga de un lugar a otro de la célula. Es un trabajo que requiere precisión tanto de espacio como de tiempo en la entrega”, dice el investigador.
El último trabajo del equipo realizado en el IBCN y en colaboración con el departamento de Física de la UBA y la Universidad de California en San Diego fue publicado en el Journal of Cell Science y demuestra cómo el transporte rápido del proteasoma depende de la asociación a diferentes cargas axonales y de la actividad de los motores moleculares para viajar a través del axón.
“Mediante el diseño y la utilización de cargas fluorescentes describimos las propiedades de transporte de partículas únicas del proteasoma junto a diferentes vesículas y organelas a lo largo del axón. Estas propiedades de movimiento, son utilizadas para identificar el rol de las mismas en la iniciación y progresión de patologías que se generan por defectos del transporte axonal”, detalla Maria Gabriela Otero, integrante del grupo de investigación.
De esta manera, los científicos hicieron que el proteasoma luciera fluorescente y mediante un sistema de alta resolución espacio-temporal y algoritmos lograron localizar partículas únicas e identificar cuáles son sus dinámicas de movimiento.
“Caracterizamos proteasomas que se mueven rápido, porque se asocian a cargas que dependen de proteínas motoras; otros que difunden libremente en el axón; y observamos también un tercer tipo, que se mueve de manera confinada. Es decir que tienen determinada cuota de movimiento pero no son liberados para el transporte” aclara Falzone.
(Click en la imagen para agrandar)
El proteasoma y el transporte activo
El interés de este trabajo se centró específicamente en los proteasomas que se mueven rápido, o sea, los que tienen un transporte activo desde el cuerpo celular a la sinapsis.
“Hemos comprobado que el proteasoma se asocia a membranas de diferentes vesículas u organelas y así emprende su viaje a través de la célula” explica Otero, quien agrega que los resultados de la investigación muestran que el proteasoma necesita asociarse a otra estructura para moverse y migrar desde el cuerpo celular a la sinapsis.
De esta manera han atisbado una primera descripción de cómo este sistema de degradación se traslada, una función muy relevante para eliminar proteínas que están asociadas con las enfermedades neurodegenerativas. Según los investigadores del trabajo surgen interrogantes acerca de si existen alteraciones en las dinámicas de movimiento de este complejo que podrían explicar patologías como el Alzheimer, una enfermedad que empieza localmente en la sinapsis con acumulación de proteínas que no pueden degradadas, ya sea por una mala señalización o porque el sistema de degradación, el proteasoma, no se encuentra presente. “Aun queda mucho por resolver”, concluye Falzone.
- Por: Jimena Naser
- Sobre Investigación:
- Tomás Falzone. Investigador adjunto. Instituto de Biología Celular y Neurociencias.
- María Gabriela Otero. UBA.