Ciencias Biológicas y de la Salud
La importancia de antagonistas de la progesterona en el tratamiento del cáncer de mama
Investigadores del CONICET y médicos del Hospital Zonal General de General Pacheco estudian una terapia con un antiprogestágeno para inhibir el crecimiento tumoral.
Los estrógenos y la progesterona son hormonas femeninas producidas por los ovarios. Los primeros están involucrados en el desarrollo de las características sexuales femeninas, mientras que la segunda tiene un rol fundamental en el ciclo menstrual y en el embarazo ya que prepara al útero para la recepción del óvulo fecundado. Pero, además, estas hormonas promueven el crecimiento de algunos tipos de cáncer de mama.
Las células tumorales sensibles a las hormonas contienen proteínas que se conocen como receptores de hormonas que se activan cuando los estrógenos y la progesterona se unen a ellas y, de esta manera, estimulan por ejemplo, la proliferación celular. Teniendo en cuenta esto, las terapias en el cáncer de mama de tipo hormonal existentes tienen como blanco terapéutico a los estrógenos y sus receptores.
Desde hace más de una década, en el laboratorio de ‘Carcinogénesis Hormonal’ del Instituto de Biología y Medicina Experimental (IBYME, CONICET-FIBYME) dirigido por Claudia Lanari, investigadora superior del CONICET, focalizan sus estudios en investigar los receptores de progesterona y su participación en el crecimiento tumoral.
En un estudio recientemente publicado en la revista Journal of the National Cancer Institute (JNCI) Lanari estudió junto a su equipo cómo se comportan dos isoformas –diferentes formas en que se presentan las moléculas de una proteína- del receptor de progesterona (RP): la A (RPA) y la B (RPB) frente al desarrollo tumoral.
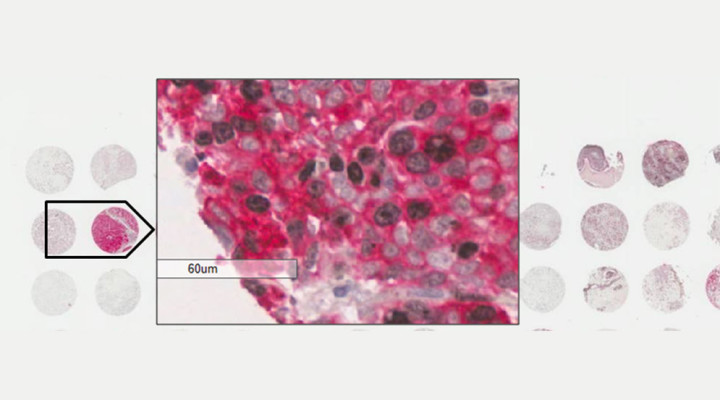
Esta investigación es producto de más de 10 años de trabajo. Comenzó con estudios en ratones y cultivos celulares para luego confirmar esos resultados en muestras humanas. Para ello, realizaron cultivos de tejido de tumores ex vivo (fuera del organismo) de pacientes con cáncer de mama del Hospital Zonal General de Agudos “Magdalena Villegas de Martínez” de General Pacheco que fueron tratados con un antiprogestágeno, es decir un compuesto que contrarresta la acción del progestágeno. Al mismo tiempo evaluaron la expresión de las isoformas del RP del tumor. Lo que observaron fue que los tumores que se inhiben con un antiprogestágeno son aquellos con una mayor proporción de RPA que de RPB.
“Con estos resultados podemos decir, que los pacientes que presentan una mayor cantidad de isoforma A que de isoforma B podrían beneficiarse de una terapia con antiprogestágenos”, explica Paola Rojas, investigadora asistente del CONICET en IBYME y autora principal del estudio.
“Cuando una paciente va al hospital y detectamos un tumor, una de las primeras acciones es sacarlo mediante cirugía. Cuando pasa esto, le avisamos al equipo de Lanari y se acerca alguien con hielo seco y un frasco con medio de cultivo para tomar la muestra. Por un lado se cultiva, le hacen un tratamiento de 48 horas con el antiprogestágeno y por otro lado se hace un estudio para ver su perfil de isoformas. La manipulación de las muestras requiere de cuidados para evitar errores. El tumor sin vascularización se muere, y la muestra en hielo no tiene que perder el frío, por lo que se debe trasladar, rápidamente al Laboratorio para procesarla”, advierte Hugo Gass, cirujano consultor de ese hospital.
El antiprogestágeno que decidieron utilizar los especialistas es la mifepristona, un compuesto de origen francés que era utilizado como anticonceptivo de emergencia y actualmente se suministra para el tratamiento de la enfermedad de Cushing, una patología caracterizada por el exceso crónico de cortisol.
“En este caso la vamos a usar para el tratamiento del cáncer de mama, y entonces uno de los requisitos para cuando reclutamos las pacientes es que sean postmenopáusicas para evitar un posible aborto. Pero no es una droga que se tuvo que elaborar y eso es muy bueno porque todas las drogas para el cáncer llevan un largo proceso y son inaccesibles en cuestión de precios. Tuvimos que importar la mifepristona de Canadá, y fue un proceso muy largo y engorroso pero está en el mercado y es económica”, agrega Rojas.
El futuro de los ensayos
Actualmente, luego de los exitosos resultados publicados, los profesionales del Laboratorio de Lanari junto a Hugo Gass trabajan en un ensayo clínico de la mifepristona como neoadyuvante, esta vez directamente en pacientes con cáncer de mama para estudiar los efectos de la droga sobre el tumor en un breve período.
“Hubo un concurso del Ministerio de Ciencia, Tecnología e Innovación Productiva de la Nación hace 4 años para presentar proyectos de investigación de impacto en la comunidad y nos presentamos. Con el subsidio estamos llevando a cabo este ensayo que consiste en el uso de la mifepristona antes de iniciar el tratamiento convencional cuya primera acción es la cirugía. Durante 14 días le administramos una pastilla de 200 mg del antiprogestágeno y en el día 15 se opera. El día que la paciente viene a la consulta y con una biopsia confirmamos que tiene cáncer, parte de la muestra se manda a analizar al Laboratorio de Lanari para estudiar si tiene sobreexpresada la isoforma RPA y, si califica, se informa al hospital. Se hacen estudios y se adecua la agenda quirúrgica porque la operación no se pude posponer”, explica Gass.
El médico aclara que el reclutamiento de voluntarias del tratamiento tiene varios criterios de exclusión como que la paciente sea postmenopaúsica, que no sea asmática, no tenga enfermedades severas, ni haya tenido ningún tipo de cáncer previo. Para el seguimiento de estos ensayos, hay un oncólogo, becario doctoral del proyecto, de forma permanente en el hospital dedicado a las pacientes y encargado de todo el protocolo.
Por su parte, Lanari advierte que es importante entender que este tratamiento no es un beneficio directo a la persona que lo recibe sino un trabajo de investigación. Es una ayuda potencial para pacientes a futuro y no le trae ningún problema. “Si esta droga es útil tenemos un arma más para vencer el cáncer de mama, económica y sin efectos secundarios”, asegura.
Estudios moleculares
Las muestras de pacientes clasificadas en isoforma RPA y RPB se enviaron al laboratorio de Charles Perou en Estados Unidos, un reconocido investigador que propuso la clasificación molecular de los tumores de mama basado en la secuenciación de ARN, una tecnología que se está usando para poder encontrar nuevas mutaciones o alteraciones que puedan orientar al desarrollo de tratamientos dirigidos.
Finalmente, Martín Abba, investigador independiente del CONICET en el Centro de Investigaciones Inmunológicas Básicas y Aplicadas de la Universidad de La Plata (CINIBA) fue quien encontró una relación entre la clasificación molecular de los tumores de mama y la mayor expresión de una isoforma que de la otra. Esa relación de isoformas se puede utilizar como un marcador pronóstico para la enfermedad.
“Si hay más de una isoforma que de la otra (RPA mayor que RPB) quiere decir que la paciente podría tener un mejor futuro porque el tumor es menos agresivo que cuando la proporción es inversa. Hasta este momento no se sabía y más bien se pensaba lo contrario. Como los tratamientos con antiestrógenos son muy efectivos, se demoró el interés en estudiar lo que pasa con la progesterona como protagonista. Con el tiempo si esto llega a prosperar la idea es poder combinar la mifepristona con los antiestrógenos, la idea no es reemplazar si no complementar”, concluye Lanari.
Para ver el video haga click aquí.
Por Cecilia Leone.
Sobre investigación:
Claudia Lanari. Investigadora superior. IBYME.
Paola Rojas. Investigadora asistente. IBYME.
Gonzalo Sequeira. Becario posdoctoral. IBYME.
Andrés Elia. Beca de estudiantes. IBYME.
Martín Abba. Investigador independiente. CINIBA.
María May. Becaria doctoral (hasta 2016). IBYME.
Michelle Álvarez. Becaria (hasta 2016). IBYME.
Paula Martínez. Hospital Zonal General de agudos “Magdalena Villegas de Martínez”.
Pedro González. Hospital Zonal General de agudos “Magdalena Villegas de Martínez”.
Sthephen Hewitt. National Institutes of Health. EE. UU.
Xiaping He. National UNC, Chapel Hill. EE. UU.
Charles M. Perou. UNC, Chapel Hill. EE. UU.
Alfredo Molinolo. Moores Cancer Center. San Diego, EE. UU.
Luz Gibbons. Instituto de efectividad clínica y sanitaria.
Hugo Gass. Hospital Zonal General de agudos “Magdalena Villegas de Martínez”.